ਪਾਣੀ ਦੇ ਗੁਣ: ਆਈਸੋਟੋਪਸ ਅਤੇ ਅਣੂ ਬਣਤਰ.
ਪਾਣੀ ਦੇ ਗੁਣ 1: ਆਮ
ਪਾਣੀ 2 ਦੇ ਗੁਣ: ਸਰੀਰਕ ਅਤੇ ਰਸਾਇਣਕ ਗੁਣ
ਪਾਣੀ ਦੀ ਆਈਸੋਟੋਪਿਕ ਰਚਨਾ
ਪਾਣੀ ਆਕਸੀਜਨ ਅਤੇ ਹਾਈਡ੍ਰੋਜਨ ਆਈਸੋਟੋਪਸ ਦੇ ਨਿ combਕਲੀਅਸ ਵਿਚ ਪ੍ਰੋਟੋਨ ਨਾਲ ਜੁੜੇ ਨਿ neutਟ੍ਰੋਨ ਦੀ ਸੰਖਿਆ ਵਿਚ ਇਕ ਦੂਜੇ ਤੋਂ ਵੱਖਰੇ ਵੱਖਰੇ ਸੰਜੋਗਾਂ ਦਾ ਮਿਸ਼ਰਣ ਹੈ.
1H,2 ਐਚ (ਡਾਇਟ੍ਰੀੂਅਮ)3ਐਚ (ਟ੍ਰਿਟਿਅਮ)
16O, 17O,18O.
ਆਈਸੋਟਿਕ ਅਨੁਪਾਤ ਹੇਠ ਲਿਖੇ ਅਨੁਸਾਰ ਹਨ:
ਹਾਈਡ੍ਰੋਜਨ ਲਈ:
2H/1H = 1 / 6900
3H/1H = 1 / 10 18
ਟ੍ਰਿਟੀਅਮ ਇੱਕ ਅਸਥਿਰ ਤੱਤ ਹੈ, ਇਸਦਾ ਅੱਧ ਜੀਵਨ 12,5 ਸਾਲ ਹੈ.
ਆਕਸੀਜਨ ਲਈ:
18O/16ਹੇ = 1 / 500
17O/16ਹੇ = 1 / 2500
ਮੁੱਖ 4 ਅਣੂ ਦੀ ਕਿਸਮ ਅਤੇ ਉਨ੍ਹਾਂ ਦੇ ਆਵਿਰਤੀ ਹੇਠ ਲਿਖੇ ਅਨੁਸਾਰ ਹਨ:
1H216ਹੇ = 99,7%
1H2 18 ਹੇ = 0,2%
1H217ਹੇ = 0,04%
1HD16ਹੇ = 0,03%
D216ਹੇ = ਬਹੁਤ ਕਮਜ਼ੋਰ
ਵੱਖੋ-ਵੱਖਰੇ ਆਈਸੋਟੈਪ ਵਿਚਲੇ ਅਣੂ ਦੇ ਭੌਤਿਕ ਗੁਣਾਂ ਵਿਚ ਅੰਤਰ ਪੈਦਾ ਕਰਦੇ ਹਨ, ਖਾਸ ਤੌਰ ਤੇ ਉਨ੍ਹਾਂ ਦੀ ਘਣਤਾ, ਪਰ ਰਸਾਇਣਕ ਵਿਸ਼ੇਸ਼ਤਾਵਾਂ ਇਕਸਾਰ ਹੀ ਰਹਿੰਦੀਆਂ ਹਨ.
ਭਾਰੀ ਪਾਣੀ ਡੀ2ਓ ਇਸ ਦੀ ਕੁਦਰਤੀ ਅਵਸਥਾ ਵਿਚ ਮੌਜੂਦ ਹੈ ਪਰ ਬਹੁਤ ਵਿਚ
ਘੱਟ. ਇਸ ਦੀ ਇੱਕ ਪ੍ਰਸੰਸਾਯੋਗ ਮਾਤਰਾ ਪ੍ਰਾਪਤ ਕਰਨ ਲਈ, ਆਈਸੋਟੌਪ ਤੋਂ ਵੱਖ ਹੋਣ ਦੀਆਂ ਤਕਨੀਕਾਂ ਵਿੱਚ ਮੁਹਾਰਤ ਹਾਸਲ ਕਰਨੀ ਜ਼ਰੂਰੀ ਹੈ: ਪਰਮਾਣੂ ਹਥਿਆਰ ਨੂੰ ਤਿਆਰ ਕਰਨ ਲਈ ਆਖਰੀ ਵਿਸ਼ਵ ਯੁੱਧ ਦੌਰਾਨ ਇਹ ਬੁਨਿਆਦੀ ਚੁਣੌਤੀਆਂ ਵਿੱਚੋਂ ਇੱਕ ਸੀ.
ਪਾਣੀ ਦੇ ਰਸਾਇਣਕ ਹਿੱਸਿਆਂ ਦੇ ਆਈਸੋਟੋਪਿਕ ਰਚਨਾ ਦੀ ਵਰਤੋਂ ਥਰਮੋਡਾਇਨਾਮਿਕ ਪੈਰਾਮੀਟਰ ਜਿਵੇਂ ਕਿ ਤਾਪਮਾਨ ਦੇ ਅਨੁਮਾਨ ਵਿੱਚ ਕੀਤੀ ਜਾਂਦੀ ਹੈ;
ਰਿਪੋਰਟ 18 O/16O ਪੋਲਰ ਟੋਪੀਆਂ ਤੋਂ ਆਈਸ ਅਤੇ ਜੈਵਿਕ ਧਰਤੀ ਹੇਠਲੇ ਪਾਣੀ ਪਿਛਲੇ ਸਮੇਂ ਦੇ ਮੌਸਮ ਬਾਰੇ ਜਾਣਕਾਰੀ ਪ੍ਰਦਾਨ ਕਰਦੇ ਹਨ.
ਸਮੁੰਦਰ ਦੇ ਪਾਣੀ ਦਾ ਭਾਫ਼ ਬਣਨ ਆਈਸੋਟੋਪਿਕ ਭੰਜਨ ਦੇ ਨਾਲ ਹੁੰਦਾ ਹੈ: ਆਕਸੀਜਨ ਦਾ ਹਲਕਾ ਆਈਸੋਟੋਪ ਭਾਰੀ ਆਈਸੋਟੋਪ ਦੀ ਤਰਜੀਹ ਵਿੱਚ ਭਾਫ ਬਣ ਜਾਂਦਾ ਹੈ. ਬੱਦਲਾਂ ਅਤੇ ਮੀਂਹ ਦੇ ਪਾਣੀ ਨਾਲੋਂ ਸਮੁੰਦਰ ਭਾਰੀ ਆਈਸੋਟੋਪਾਂ ਵਿੱਚ ਅਮੀਰ ਹਨ.
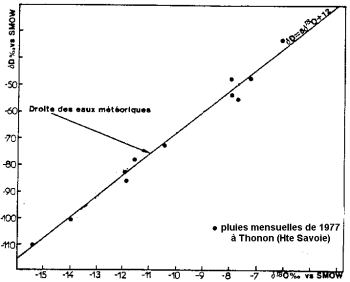
ਬਰਸਾਤ ਦੀ ਸਥਿਰ ਆਈਸੋਟੋਪ ਸਮੱਗਰੀ (ਬਲੇਵੌਕਸ ਅਤੇ ਲੈਟੋਲੇ, 1995 ਤੋਂ ਬਾਅਦ).
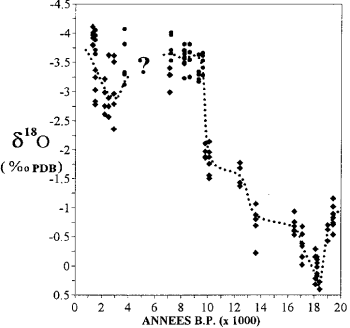
ਮਯੋਟੇ ਵਿਚ ਕੋਰਨਾਂ ਵਿਚ ਆਕਸੀਜਨ ਆਈਸੋਟੋਪ ਦੀ ਸਮੱਗਰੀ ਵਿਚ ਤਬਦੀਲੀ (ਕੈਸੈਨੋਵਾ ਐਟ ਅਲ. 1994 ਤੋਂ ਬਾਅਦ).
ਅਣੂ ਦੀ ਢਾਂਚਾ
ਹਾਈਡ੍ਰੋਜਨ ਅਤੇ ਆਕਸੀਜਨ ਪਰਮਾਣੂ ਆਪਣੇ ਇਲੈਕਟ੍ਰਾਨਾਂ ਨੂੰ ਨੀਨ ਦੀ ਤਰ੍ਹਾਂ ਇਕ ਪੂਰੀ ਪਰਤ ਬਣਾਉਂਦੇ ਹਨ. ਦਰਅਸਲ, ਆਕਸੀਜਨ ਪਰਮਾਣੂ ਕੋਲ ਇਸਦੇ ਇਲੈਕਟ੍ਰਾਨਿਕ ਸ਼ੈੱਲ ਨੂੰ ਪੂਰਾ ਕਰਨ ਲਈ 2 ਇਲੈਕਟ੍ਰੋਨ ਦੀ ਘਾਟ ਹੈ, ਇਹ 2 ਹਾਈਡ੍ਰੋਜਨ ਪਰਮਾਣੂ ਹਨ ਜੋ ਇਸਨੂੰ ਪ੍ਰਦਾਨ ਕਰਦੇ ਹਨ. ਬਣਾਇਆ ਗਿਆ H2O ਅਣੂ ਸਥਿਰ ਹੈ.
ਆਕਸੀਜਨ: 8 ਪ੍ਰੋਟੋਟ + 8 ਨਿਊਟ੍ਰੋਨ
ਹਾਈਡ੍ਰੋਜਨ: 2 (2 * (1 ਪ੍ਰੋਟੋਨ + 1 ਨਿਊਟਰਨ))
ਕੁੱਲ: 10 ਪ੍ਰੋਟੋਨ 10 ਇਲੈਕਟਰੋਨ ਦੇ ਖਰਚੇ ਨੂੰ ਸੰਤੁਲਿਤ ਕਰਦਾ ਹੈ.
ਹਾਈਡਰੋਜਨ ਨਿ nucਕਲੀ ਆਕਸੀਜਨ ਦੇ ਇੱਕ ਪਾਸੇ ਵਿਵਸਥਿਤ ਕੀਤੀ ਜਾਂਦੀ ਹੈ ਤਾਂ ਜੋ ਇੱਕ ਮਿਕੀ ਦਾ ਸਿਰ (ਹਾਈਡਰੋਜਨ ਕੰਨ ਹੋਣ) ਦੀ ਵਿਸ਼ੇਸ਼ਤਾ ਬਣਾਈ ਜਾ ਸਕੇ.
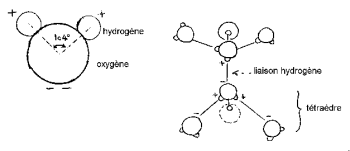
ਐਚਓਐਚ ਕੋਣ 104,474 ° (ਟੈਟਰਾਹੇਡ੍ਰਲ ਜਿਓਮੈਟਰੀ ਦੀ ਵਿਸ਼ੇਸ਼ਤਾ) ਹੈ. ਆਕਸੀਜਨ ਅਤੇ ਹਾਈਡ੍ਰੋਜਨ ਪਰਮਾਣੂ ਦੇ ਵਿਚਕਾਰ ਦੀ ਦੂਰੀ ਭਾਫ਼ ਵਿਚ 1 ਏ ° (0,95718 ਏ °) ਦੇ ਨੇੜੇ ਹੈ. ਅਣੂ ਦਾ ਪ੍ਰਭਾਵਸ਼ਾਲੀ ਵਿਆਸ 2,82 ਏ ° ਦੇ ਕ੍ਰਮ ਦਾ ਹੈ.
ਇਸ ਛੋਟੇ ਛੋਟੇ ਅਣੂ ਵਿੱਚ ਇਲੈਕਟ੍ਰਿਕ ਚਾਰਜ ਅਸਮਾਨਤ ਤੌਰ ਤੇ ਵੰਡੇ ਜਾਂਦੇ ਹਨ. ਹਾਈਡ੍ਰੋਜਨ ਪਰਮਾਣੂ ਨਾਲੋਂ ਇਲੈਕਟ੍ਰਾਨ ਵਧੇਰੇ ਆਕਸੀਜਨ ਪਰਮਾਣੂ ਵੱਲ ਖਿੱਚੇ ਜਾਂਦੇ ਹਨ. ਹਾਈਡ੍ਰੋਜਨ ਨਿleਕਲੀ ਦੇ ਨੇੜੇ ਸਕਾਰਾਤਮਕ ਚਾਰਜ ਦੇ 2 ਕੇਂਦਰ ਅਤੇ ਆਕਸੀਜਨ ਨਿleਕਲੀਅਸ ਦੇ ਨੇੜੇ ਨਕਾਰਾਤਮਕ ਚਾਰਜ ਦੇ 2 ਕੇਂਦਰ ਹਨ. ਖਰਚਿਆਂ ਦੀ ਵੰਡ ਵਿਚ ਇਹ ਅਸੰਤੁਲਨ, ਪਾਣੀ ਦੇ ਅਣੂ ਦੀ ਰੇਖਿਕ ਰੇਖਾ-ਭੂਮੀ ਦੇ ਨਾਲ ਮਿਲ ਕੇ, ਇਕ ਮਜ਼ਬੂਤ ਇਲੈਕਟ੍ਰਿਕ ਡੀਪੋਲ ਪਲ ਦੀ ਮੌਜੂਦਗੀ ਵਿਚ ਆਪਣੇ ਆਪ ਨੂੰ ਪ੍ਰਗਟ ਕਰਦਾ ਹੈ. ਪਾਣੀ ਦਾ ਅਣੂ ਧਰੁਵੀ ਹੈ; ਇਹ ਇਕ ਇਲੈਕਟ੍ਰਿਕ ਡੀਪੋਲ ਵਰਗਾ ਵਿਹਾਰ ਕਰਦਾ ਹੈ ਜੋ ਇਸ ਤਰਾਂ ਹੋਰ ਪੋਲਰ ਦੇ ਅਣੂਆਂ ਨਾਲ ਜੋੜ ਸਕਦਾ ਹੈ. ਦਰਅਸਲ, ਪਾਣੀ ਦੇ ਅਣੂ ਕ੍ਰਿਸਟਲ ਦੇ ਸੰਵਿਧਾਨਕ ਆਯੋਨਾਂ ਦੇ ਵਿਚਕਾਰ ਪਾਏ ਜਾ ਸਕਦੇ ਹਨ ਜਦੋਂ ਕਿ ਉਨ੍ਹਾਂ ਦੇ ਉਲਟ ਇਲੈਕਟ੍ਰਿਕ ਚਾਰਜ ਦੇ ਆਪਣੇ ਹਿੱਸੇ ਨੂੰ ਉਨ੍ਹਾਂ ਵੱਲ ਭੇਜਦੇ ਹਨ. ਕ੍ਰਿਸਟਲ ਲਾਈਨ ਦੇ ਆਯੋਜਨ ਦਾ ਆਕਰਸ਼ਣ ਬਹੁਤ ਕਮਜ਼ੋਰ ਹੋ ਜਾਂਦਾ ਹੈ ਅਤੇ ਕ੍ਰਿਸਟਲ ਦਾ ਏਕਤਾ ਘੱਟ ਜਾਂਦਾ ਹੈ, ਜੋ ਇਸ ਦੇ ਭੰਗ ਦੀ ਸਹੂਲਤ ਦਿੰਦਾ ਹੈ. ਪਾਣੀ ਦੇ ਅਣੂ ਦੀਆਂ ਧਰੁਵੀ ਵਿਸ਼ੇਸ਼ਤਾਵਾਂ ਮਾਈਕ੍ਰੋਵੇਵ ਹੀਟਿੰਗ ਦੀ ਤਕਨੀਕ ਬਾਰੇ ਦੱਸਦੀਆਂ ਹਨ. ਦਰਅਸਲ, ਇਕ ਧਰੁਵੀ ਅਣੂ ਇਕ ਇਲੈਕਟ੍ਰਿਕ ਖੇਤਰ ਦੇ ਸੰਬੰਧ ਵਿਚ ਆਪਣੇ ਆਪ ਨੂੰ orਾਲਦਾ ਹੈ; ਜੇ ਇਹ ਬਦਲਦਾ ਹੈ, ਅਣੂ ਸਥਿਤੀ ਦੇ ਪਰਿਵਰਤਨ ਦੀ ਪਾਲਣਾ ਕਰਦਾ ਹੈ. ਇੱਕ ਨਿਸ਼ਚਤ ਬਾਰੰਬਾਰਤਾ ਤੋਂ, ਪਾਣੀ ਲਈ ਕੁਝ ਗੀਗਾਹਰਟਜ਼, ਅਣੂਆਂ ਦੀ ਹਰਕਤ ਰਗੜ ਦੁਆਰਾ ਗਰਮੀ ਪੈਦਾ ਕਰਦੀ ਹੈ. ਘਰੇਲੂ ਤੰਦੂਰ ਆਮ ਤੌਰ 'ਤੇ 2,45 ਗੀਗਾਹਰਟਜ਼ ਦੀ ਬਾਰੰਬਾਰਤਾ' ਤੇ ਕੰਮ ਕਰਦੇ ਹਨ, ਜੋ ਯੂ.ਐੱਚ.ਐੱਫ.
ਅਣੂ ਦੇ 3 ਨਿleਕਲੀਅਸ ਸਥਿਰ ਨਹੀਂ ਹੁੰਦੇ, ਉਹ ਇਕ ਦੂਜੇ ਦੇ ਮੁਕਾਬਲੇ ਚਲਦੇ ਰਹਿੰਦੇ ਹਨ, ਅਣੂ ਕੰਬਦਾ ਅਤੇ ਮਰੋੜਦਾ ਹੈ. ਤਰਲ ਪਾਣੀ ਵਿੱਚ, ਅਣੂ ਇੱਕਠੇ ਹੁੰਦੇ ਹਨ: ਮਿਕੀ ਦੇ ਸਿਰ ਬੰਧਨ ਦੇ ਕੰਨ ਨੂੰ ਹਾਈਡਰੋਜਨ ਬੌਂਡਿੰਗ ਦੁਆਰਾ ਠੋਡੀ ਤੱਕ ਜੋੜਦੇ ਹਨ. ਦਰਅਸਲ, ਆਕਸੀਜਨ ਦੇ 8 ਪੈਰੀਫਿਰਲ ਇਲੈਕਟ੍ਰਾਨਾਂ ਵਿਚੋਂ, ਸਿਰਫ 4 ਹਾਈਡ੍ਰੋਜਨ ਪਰਮਾਣੂਆਂ ਦੇ ਸਹਿਜ ਬਾਂਡਾਂ ਵਿਚ ਸ਼ਾਮਲ ਹਨ. ਬਾਕੀ 4 ਇਲੈਕਟ੍ਰਾਨਾਂ ਨੂੰ 2 ਜੋੜਿਆਂ ਵਿੱਚ ਵੰਡਿਆ ਜਾਂਦਾ ਹੈ ਜਿਸ ਨੂੰ ਮੁਫਤ ਇਲੈਕਟ੍ਰੌਨ ਡਬਲਟਸ ਕਹਿੰਦੇ ਹਨ. ਇਹ ਹਰ ਨਾਕਾਰਾਤਮਕ ਇਲੈਕਟ੍ਰਿਕ ਚਾਰਜਡ ਡਬਲਜ਼ ਇਕ ਨੇੜਲੇ ਪਾਣੀ ਦੇ ਅਣੂ ਤੋਂ ਸਕਾਰਾਤਮਕ ਚਾਰਜਡ ਹਾਈਡ੍ਰੋਜਨ ਐਟਮ ਨਾਲ ਇਕ ਇਲੈਕਟ੍ਰੋਸਟੈਟਿਕ ਬਾਂਡ ਬਣਾ ਸਕਦਾ ਹੈ. ਹਾਈਡ੍ਰੋਜਨ ਬਾਂਡ, ਜੋ ਕਿ ਕਮਰੇ ਦੇ ਤਾਪਮਾਨ ਤੇ ਸਥਿਰ ਹੁੰਦਾ ਹੈ, ਫਿਰ ਵੀ ਸਹਿਭਾਗੀ ਬਾਂਡ ਦੇ ਮੁਕਾਬਲੇ ਕਮਜ਼ੋਰ ਹੁੰਦਾ ਹੈ. ਪਾਣੀ ਦੇ ਅਣੂ ਵਿਚ, 2 ਕੋਵਲੈਂਟ ਬਾਂਡਾਂ ਅਤੇ 2 ਫ੍ਰੀ ਇਲੈਕਟ੍ਰਾਨਿਕ ਡਬਲਜ਼ ਦੀ ਦਿਸ਼ਾ ਦੁਆਰਾ ਬਣਾਈ ਗਈ ਰੇਖਾ-ਭੂਮੀ ਇਕ ਟੈਟਰਾਹੇਡ੍ਰੋਨ ਦੇ ਨੇੜੇ ਹੈ ਜਿਸ ਦੇ ਕੇਂਦਰ ਵਿਚ ਆਕਸੀਜਨ ਨਿ nucਕਲੀ ਦਾ ਕਬਜ਼ਾ ਹੈ.
ਹਾਲਾਂਕਿ, ਪਾਣੀ ਦੇ ਅਣੂ ਦਾ ਵੱਡਾ structureਾਂਚਾ ਅਜੇ ਵੀ ਨਾਮੁਕੰਮਲ ਤੌਰ ਤੇ ਜਾਣਿਆ ਜਾਂਦਾ ਹੈ. ਐਕਸ-ਰੇ ਅਤੇ ਨਿ neutਟ੍ਰੋਨ ਵਿਛੋੜਾ ਸਪੈਕਟ੍ਰਾ 2 ਮੁੱਖ ਮੁੱਲਾਂ ਪ੍ਰਦਾਨ ਕਰਦੇ ਹਨ: 1 ਏ to ਨਾਲ ਸੰਬੰਧਿਤ ਇਕ ਸੰਕੇਤ, ਹਾਈਡ੍ਰੋਜਨ ਅਤੇ ਆਕਸੀਜਨ ਨਿiਕਲੀ ਦੇ ਵਿਚਕਾਰ ਦੀ ਦੂਰੀ, ਅਤੇ ਤਾਪਮਾਨ ਦੇ ਅਨੁਸਾਰ ਵੱਖਰੇ ਵੱਖਰੇ 2,84 ਤੋਂ 4 ਏ value ਦਾ ਮੁੱਲ ਅਤੇ 2 ਆਕਸੀਜਨ ਨਿ nucਕਲੀ ਦੇ ਵਿਚਕਾਰ ਦੀ ਦੂਰੀ ਦੇ ਅਨੁਸਾਰੀ. ਐਕਸ-ਰੇ ਡਿਫ੍ਰੈਕਟੋਮੀਟਰੀ ਕਿਸੇ ਨਿਰਮਾਣ ਅਣੂ ਤੋਂ ਦੂਰੀ 'ਤੇ ਸਥਿਤ ਤਰਲ ਦੀ ਪ੍ਰਤੀ ਯੂਨਿਟ ਵਾਲੀਅਮ ਦੇ ਅਣੂਆਂ ਦੀ numberਸਤ ਗਿਣਤੀ ਨੂੰ ਜਾਣਨਾ ਵੀ ਸੰਭਵ ਬਣਾਉਂਦੀ ਹੈ. ਪਾਣੀ ਦੇ ਅਣੂ ਵਿਚ 4,4.ਸਤਨ 4 ਗੁਆਂ neighborsੀ ਹੁੰਦੇ ਹਨ, ਜੋ ਇਕ ਟੈਟਰਾਹੇਡ੍ਰਲ ਜਾਲ ਦਾ ਸੁਝਾਅ ਦਿੰਦੇ ਹਨ. ਹਾਈਡ੍ਰੋਜਨ ਬਾਂਡ ਨਾਲ ਜੁੜੇ ਅਣੂਆਂ ਤੋਂ ਇਲਾਵਾ, ਹੋਰ ਅਣ-ਮਾਤਰ ਅਣੂ ਹਨ, ਜੋ ਦੱਸ ਸਕਦੇ ਹਨ ਕਿ ਕਿਉਂ ਗੁਆਂ neighboringੀ ਅਣੂਆਂ ਦੀ ਗਿਣਤੀ 4 ਤੋਂ ਥੋੜ੍ਹੀ ਹੈ, ਅਤੇ XNUMX ਬਿਲਕੁਲ ਨਹੀਂ ਜਿਵੇਂ ਕਿ ਇਕ ਸਖਤ ਟੈਟਰਾਹੇਡ੍ਰਿਕ ਕ੍ਰਿਸਟਲਾਈਜ਼ਡ ਸਟੇਟ ਲਗਾਈ ਜਾਂਦੀ ਹੈ. ਹਾਈਡ੍ਰੋਜਨ ਬਾਂਡਾਂ ਨਾਲ ਜੁੜੇ ਅਣੂਆਂ ਦਾ ਕ੍ਰਿਸਟਲ ਜਾਲੀ ਖੁਰਦ-ਬੁਰਦ ਬਣਾਏਗਾ ਜਿੱਥੇ ਅਨਬਾਉਂਡ ਅਣੂ ਰੱਖੇ ਜਾਣਗੇ. ਇਕ ਹੋਰ ਧਾਰਣਾ ਹਾਈਡ੍ਰੋਜਨ ਬਾਂਡਾਂ ਦੀ ਭਟਕਣਾ 'ਤੇ ਅਧਾਰਤ ਹੈ. ਬਾਅਦ ਦਾ, ਅਸਲ ਰੂਪ ਰੇਖਾ, ਜਿਸਦਾ ਅਰਥ ਹੈ ਓ - ਐਚ ਪਰਮਾਣੂ ਇਕਸਾਰ ਹਨ, ਵੱਖ-ਵੱਖ ਡਿਗਰੀ ਨੂੰ ਮਰੋੜ ਸਕਦੇ ਹਨ ਅਤੇ ਅਣੂਆਂ ਨੂੰ ਨੇੜੇ ਦੇ ਗੁਆਂ neighborsੀਆਂ ਨਾਲੋਂ ਕੇਂਦਰੀ ਅਣੂ ਤੱਕ ਪਹੁੰਚਣ ਦੀ ਆਗਿਆ ਦੇ ਸਕਦੇ ਹਨ.
ਸਿਧਾਂਤਕ ਨਮੂਨੇ ਹਾਲ ਹੀ ਵਿੱਚ ਸ਼ਕਤੀਸ਼ਾਲੀ ਕੰਪਿ usingਟਰਾਂ ਦੀ ਵਰਤੋਂ ਨਾਲ ਤਿਆਰ ਕੀਤੇ ਗਏ ਹਨ. ਉਹ ਸੰਕੇਤ ਦਿੰਦੇ ਹਨ ਕਿ ਲਗਭਗ 80% ਪਾਣੀ ਦੇ ਅਣੂ 3 ਜਾਂ 4 ਹਾਈਡ੍ਰੋਜਨ ਬਾਂਡਾਂ ਵਿੱਚ ਸ਼ਾਮਲ ਹੁੰਦੇ ਹਨ; ਦੂਜੇ ਪਾਸੇ, ਉਹ ਅਨਬਾ .ਂਡ ਅਣੂਆਂ ਦੀ ਮੌਜੂਦਗੀ ਨੂੰ ਬਾਹਰ ਕੱ .ਦੇ ਹਨ. ਕੰਪਿ Computerਟਰ ਮਾਡਲਿੰਗ ਸੁਝਾਅ ਦਿੰਦੀ ਹੈ ਕਿ ਜਿਵੇਂ ਜਿਵੇਂ ਪਾਣੀ ਠੰ .ਾ ਹੁੰਦਾ ਜਾ ਰਿਹਾ ਹੈ, ਅਣੂਆਂ ਦੇ ਨੈਟਵਰਕ ਵਧਦੀ ਬਰਫ਼ ਦੇ ਸਮਾਨ ਹੇਕਸਾਗਨ ਦੇ ਸਮਾਨ ਹੁੰਦੇ ਹਨ.
ਠੋਸ ਰਾਜ ਇੱਕ ਸਖਤ ਕ੍ਰਿਸਟਲਲਾਈਨ ਪ੍ਰਬੰਧ ਨਾਲ ਮੇਲ ਖਾਂਦਾ ਹੈ. ਸਧਾਰਣ ਦਬਾਅ 'ਤੇ, ਬਰਫ਼ ਦੀ ਇਕ ષोडਯੁਣੀ ਬਣਤਰ ਹੁੰਦੀ ਹੈ. ਘੱਟ ਤਾਪਮਾਨ ਤੇ (-80 ਡਿਗਰੀ ਸੈਲਸੀਅਸ ਤੋਂ ਘੱਟ), ਇਹ ਕਿ cubਬਿਕ structureਾਂਚਾ ਲੈ ਸਕਦਾ ਹੈ. ਇਲੈਕਟ੍ਰੀਕਲ ਖਰਚੇ ਕ੍ਰਿਸਟਲ ਜਾਲੀ ਵਿੱਚ ਚਲੇ ਜਾ ਸਕਦੇ ਹਨ ਅਤੇ ਆਇਯੋਨਿਕ ਕਿਸਮ ਦੇ ਕ੍ਰਿਸਟਲ ਨੁਕਸ ਪੈਦਾ ਕਰ ਸਕਦੇ ਹਨ: ਹਾਈਡਰੇਟਡ ਪ੍ਰੋਟੋਨ ਐਚ 3 ਓ + ਅਤੇ ਹਾਈਡ੍ਰੋਕਸਾਈਲ ਆਇਨ ਓਐਚ-. ਬਰਫ਼ ਦੀ ਕ੍ਰਿਸਟਲ ਜਾਲੀ ਅਣੂ ਦੇ ਸਭ ਤੋਂ ਸੰਖੇਪ ਸੰਭਾਵਤ ਸਟੈਕਿੰਗ ਨਾਲ ਸੰਬੰਧਿਤ ਨਹੀਂ ਹੈ. ਫਿusionਜ਼ਨ 'ਤੇ, ਨੁਕਸ collapseਹਿ ਜਾਂਦੇ ਹਨ ਕਿਉਂਕਿ ਹਾਈਡ੍ਰੋਜਨ ਬਾਂਡ ਟੁੱਟ ਜਾਂਦੇ ਹਨ ਅਤੇ ਅਣੂ ਇਕ ਦੂਜੇ ਦੇ ਨੇੜੇ ਆ ਜਾਂਦੇ ਹਨ: ਘਣਤਾ ਵੱਧ ਤੋਂ ਵੱਧ 4 ° ਸੈਲਸੀਅਸ ਤੱਕ ਵੱਧ ਜਾਂਦੀ ਹੈ. ਇਸਦੇ ਬਾਅਦ, ਤਰਲ ਪਾਣੀ ਵਿੱਚ, ਤਾਪਮਾਨ ਵਿੱਚ ਵਾਧਾ ਅਣੂਆਂ ਨੂੰ ਅਲੱਗ ਕਰ ਦਿੰਦਾ ਹੈ ਅਤੇ ਘਣਤਾ ਘਟਦੀ ਹੈ.
ਹੋਰ ਜਾਣਨ ਲਈ, ਹਵਾਲਾ ਅਤੇ ਬੀਬਲੀਓਗ੍ਰਾਫੀ:
ਬਲੇਵੌਕਸ ਬੀ ਅਤੇ ਲੈਟੋਲੇ ਆਰ. (1995) - ਧਰਤੀ ਹੇਠਲੇ ਪਾਣੀ ਦੇ ਗਿਆਨ ਵਿੱਚ ਆਈਸੋਟੋਪਿਕ ਤਕਨੀਕਾਂ ਦਾ ਯੋਗਦਾਨ. ਜਿਓਕ੍ਰੋਨਿਕਸ, 54, ਪੀ. 12-15.
ਕੈਰੋ ਪੀ. (1990) - ਪਾਣੀ ਦੀ ਸਰੀਰਕ ਅਤੇ ਰਸਾਇਣਕ ਵਿਸ਼ੇਸ਼ਤਾਵਾਂ. ਪਾਣੀ ਦੀ ਮਹਾਨ ਕਿਤਾਬ, ਲਾ ਵਿਲੇਟ, ਪੀ. 183-194.
ਈਗਲੈਂਡ ਡੀ (1990) - ਪਾਣੀ ਦੀ ਬਣਤਰ. ਰਿਸਰਚ, 221, ਪੀ. 548-552.
ਮੈਡਮੈਂਟ ਡੀ.ਆਰ. (1992) - ਹਾਈਡ੍ਰੋਓਲੋਜੀ ਦੀ ਕਿਤਾਬਚਾ. ਮੈਕ ਗਰੂ ਹਿੱਲ.
ਕੈਸਨੋਵਾ ਜੇ., ਕੋਲਨਾ ਐਮ ਅਤੇ ਡੀਜਰੌਡ ਕੇ. (1994) - ਜੀਓਪ੍ਰੋਸੈਕਟਿਵ - ਪਾਲੀਓਕਲੀਮੇਟੋਲੋਜੀ. ਰੈਪ. ਵਿਗਿਆਨਕ. ਬੀਆਰਜੀਐਮ, ਪੀ. 76-79.

